Zestaw Ultra HiFidelity PCR
Cechy
■ Łatwy w obsłudze: ten zestaw jest dostarczany jako 2x premiks, a PCR można przeprowadzić przez proste dodanie szablonów i starterów.
■ Wysoka wierność: wierność jest 50 razy większa niż w przypadku polimerazy Taq.
■ Wysoka specyficzność: Doskonała wydajność gorącego startu zapewniająca specyficzność produktu.
■ Szybkie wzmocnienie: Szybkość rozciągania może osiągnąć 10-15 s/kb.
■ Silna rozciągliwość: Można amplifikować fragmenty DNA do 20 kb.
■ Szerokie zastosowanie: Zestaw zawiera wzmacniacz PCR i jest odpowiedni do amplifikacji matryc o wysokim współczynniku GC i złożonych.
Specyfikacja
typu: Polimeraza DNA o wysokiej wierności
Prędkość wzmocnienia: 10-15 s/kb
Rozmiar fragmentu: <20kb
Zastosowania: amplifikacja PCR o wysokiej wierności, klonowanie genów, amplifikacja matrycy o wysokiej GC, klonowanie genów złożonych genomów, amplifikacja cDNA o wysokiej wierności, wykrywanie SNP, mutacja specyficzna dla miejsca itp.
Wydajność ekstrakcji DNA z różnych tkanek roślinnych:
Uwaga: wydajność DNA zależy od rodzaju próbki. Wszystkie powyższe materiały pochodzą z delikatnych liści.
Wszystkie produkty można dostosować do potrzeb ODM/OEM. Dla szczegółów,kliknij opcję Dostosowana usługa (ODM/OEM)
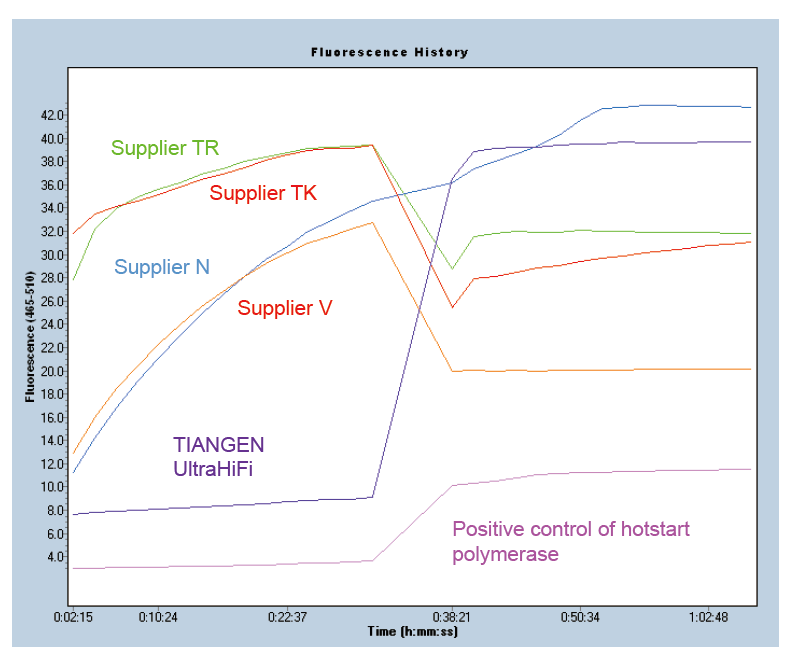 |
Gorący start w celu zapewnienia specyfiki produktu Rysunek 1. Ultra HiFi ma doskonałą funkcję gorącego startu, aby zapewnić specyficzność produktów wzmacniających. Zastosowano metodę radiolatarni molekularnych (Ma et al., Anal Biochem, 2006). |
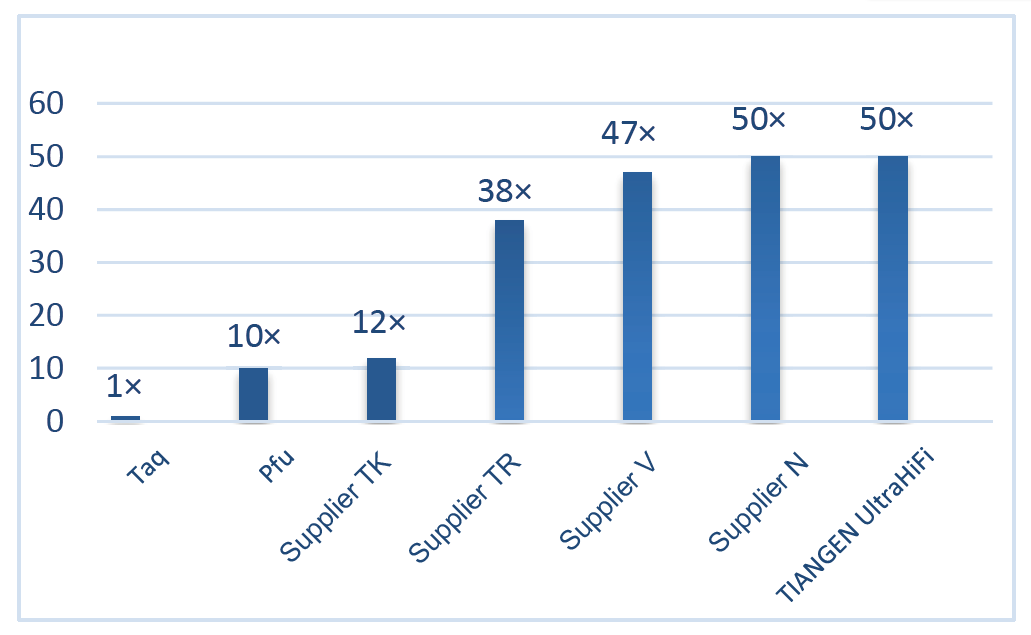 |
Doskonała wysoka wierność, 50 razy wyższa niż Taq Polymerase Rysunek 2. Wierność Ultra HiFi jest 50 razy wyższa niż w przypadku zwykłej polimerazy Taq. Jako odniesienie zastosowano wierność polimeryzacji polimerazy Taq (bez aktywności korekcyjnej). |
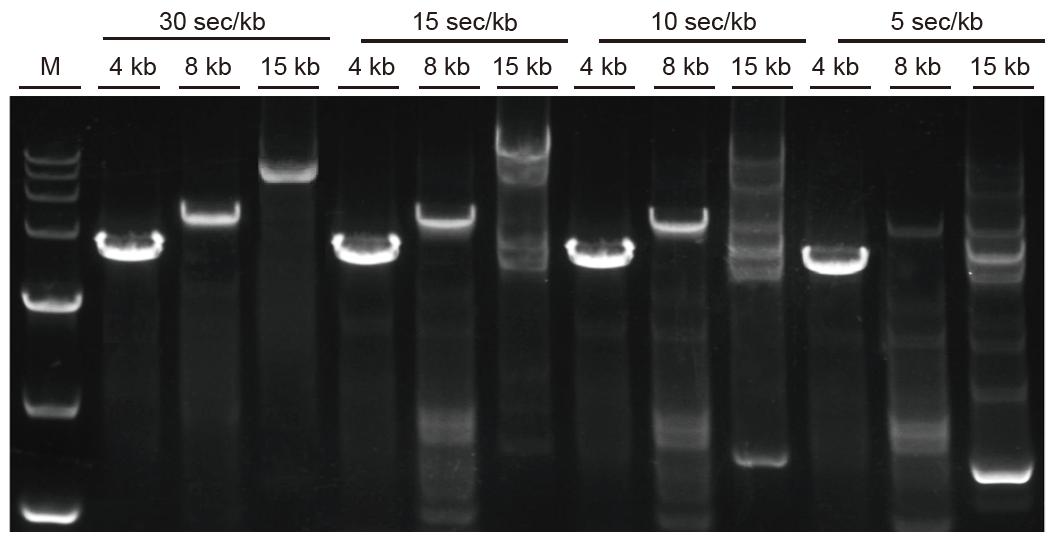 |
Szybka amplifikacja i długie fragmenty mogą być szybko amplifikowane Rys. 3. Ultra HiFi może rozciągać się do 5 s/kb dla fragmentów mniejszych niż 4 kb. W przypadku długich fragmentów czas amplifikacji można odpowiednio wydłużyć. W przypadku fragmentów większych niż 15 kb prędkość zasięgu może wynosić do 30 s/kb. M: Znacznik TIANGEN D15000 |
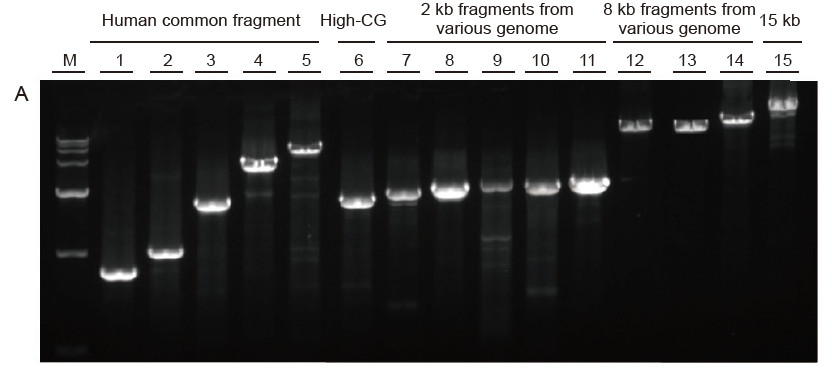 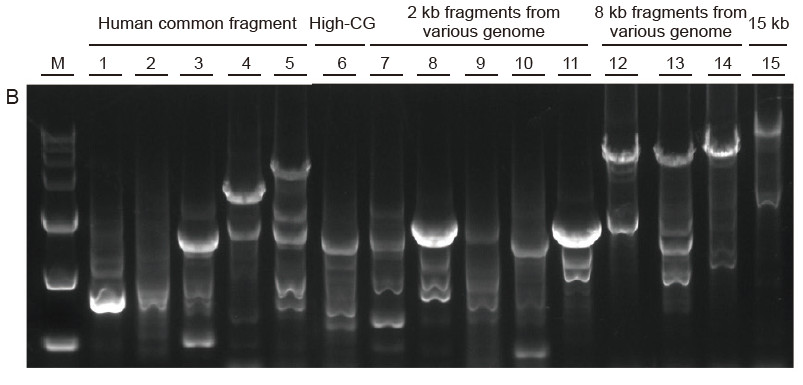 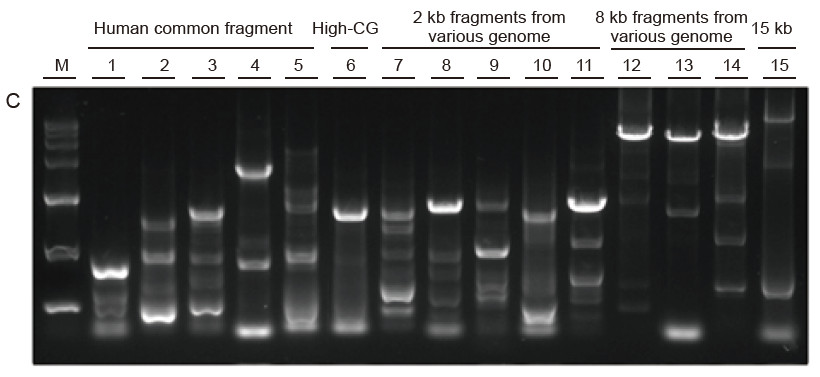 |
Silna uniwersalność i wysoka specyficzność, łatwe do odczytania wysokie GC i długie fragmenty z różnych źródeł Rysunek 4. Ultra HiFi ma wysoką specyficzność, aby zapewnić wskaźnik powodzenia amplifikacji i ilość produktu dla różnych typów szablonów. A. Wyniki wzmocnienia Ultra HiFi B. Wyniki amplifikacji enzymu Hi-Fi dostawcy K C. Wyniki amplifikacji enzymu Hi-Fi dostawcy N M: Znacznik TIANGEN D15000 Pas 1-5. Wyniki amplifikacji matryc o różnej długości: 1.750 pz; 2. 1 kb; 3. 2 kb; 4. 4 kb; 5. 6 kb Ścieżka 6. Wynik amplifikacji matrycy o wysokiej GC: 1915 pz (GC%: 70%); Pas 7-11. Wynik amplifikacji matryc 2 kb z różnych genomów: 7. Szczur; 8. Ryż; 9. Pszenica; 10. Kukurydza; 11. Bakterie; Pas 12-14. Wynik amplifikacji fragmentów o długości 8 kb: 12. Ryż; 13. Kukurydza; |
Szablon A-1
■ Matryca zawiera zanieczyszczenia białkowe lub inhibitory Taq itp. ——Oczyść matrycę DNA, usuń zanieczyszczenia białkowe lub ekstrahuj matryce DNA za pomocą zestawów do oczyszczania.
■ Denaturacja szablonu nie jest kompletna —— Odpowiednio zwiększyć temperaturę denaturacji i przedłużyć czas denaturacji.
■ Degradacja szablonu — — Ponownie przygotuj szablon.
Podkład A-2
■ Słaba jakość starterów —— Ponownie zsyntetyzuj starter.
■ Degradacja primera —— Rozdzielić primery o wysokim stężeniu do małej objętości w celu konserwacji. Unikaj wielokrotnego zamrażania i rozmrażania lub długotrwałego kriokonserwacji w temperaturze 4°C.
■ Niewłaściwe zaprojektowanie starterów (np. niewystarczająca długość startera, dimer utworzony między starterami itp.) - Przeprojektowanie starterów (unikaj tworzenia dimeru startera i struktury drugorzędowej)
A-3 Mg2+stężenie
■ Mg2+ stężenie jest zbyt niskie ——Właściwie zwiększyć Mg2+ stężenie: Optymalizacja Mg2+ stężenie poprzez serię reakcji od 1 mM do 3 mM w odstępie 0,5 mM w celu określenia optymalnego Mg2+ stężenie dla każdej matrycy i startera.
A-4 Temperatura wyżarzania
■ Wysoka temperatura annealingu wpływa na wiązanie startera i matrycy. —— Zmniejsz temperaturę wyżarzania i zoptymalizuj warunki z gradientem 2°C.
A-5 Czas przedłużenia
■ Krótki czas przedłużenia——Wydłużenie czasu przedłużenia.
Zjawiska: Próbki ujemne również wykazują prążki sekwencji docelowej.
A-1 Zanieczyszczenie PCR
■ Zanieczyszczenie krzyżowe sekwencji docelowej lub produktów amplifikacji ——Uważaj, aby nie odpipetować próbki zawierającej sekwencję docelową w próbce ujemnej ani nie wylać jej z probówki wirówkowej. Odczynniki lub sprzęt powinny być autoklawowane w celu wyeliminowania istniejących kwasów nukleinowych, a zanieczyszczenie powinno być stwierdzone poprzez eksperymenty z kontrolą ujemną.
■ Zanieczyszczenie odczynnikiem —— Podziel odczynniki i przechowuj w niskiej temperaturze.
A-2 Primer
■ Mg2+ stężenie jest zbyt niskie ——Właściwie zwiększyć Mg2+ stężenie: Optymalizacja Mg2+ stężenie poprzez serię reakcji od 1 mM do 3 mM w odstępie 0,5 mM w celu określenia optymalnego Mg2+ stężenie dla każdej matrycy i startera.
■ Niewłaściwy projekt startera i sekwencja docelowa ma homologię z sekwencją inną niż docelowa. —— Przeprojektuj podkłady.
Zjawiska: Prążki amplifikacji PCR są niezgodne z oczekiwaną wielkością, albo duże, albo małe, lub czasami występują zarówno specyficzne prążki amplifikacji, jak i nieswoiste prążki amplifikacji.
Podkład A-1
■ Słaba specyficzność startera
—— Przeprojektuj podkład.
■ Stężenie podkładu jest zbyt wysokie ——Właściwie zwiększ temperaturę denaturacji i przedłuż czas denaturacji.
A-2 Mg2+ stężenie
■ Mg2+ stężenie jest zbyt wysokie ——Właściwie zmniejsz stężenie Mg2+: Zoptymalizuj Mg2+ stężenie poprzez serię reakcji od 1 mM do 3 mM w odstępie 0,5 mM w celu określenia optymalnego Mg2+ stężenie dla każdej matrycy i startera.
A-3 Termostabilna polimeraza
■ Nadmierna ilość enzymu —— Odpowiednio zmniejsz ilość enzymu w odstępach 0,5 U.
A-4 Temperatura wyżarzania
■ Temperatura wyżarzania jest zbyt niska —— Odpowiednio zwiększyć temperaturę wyżarzania lub zastosować metodę wyżarzania dwuetapowego
A-5 cykli PCR
■ Za dużo cykli PCR —— Zmniejsz liczbę cykli PCR.
Podkład A-1——Słaba specyficzność ——Przeprojektuj starter, zmień położenie i długość startera, aby wzmocnić jego specyficzność; lub wykonaj zagnieżdżoną reakcję PCR.
A-2 Szablon DNA
—— Matryca nie jest czysta —— Oczyść matrycę lub wyodrębnij DNA za pomocą zestawów do oczyszczania.
A-3 Mg2+ stężenie
——Mg2+ stężenie jest zbyt wysokie ——Właściwie zmniejsz Mg2+ stężenie: Optymalizacja Mg2+ stężenie poprzez serię reakcji od 1 mM do 3 mM w odstępie 0,5 mM w celu określenia optymalnego Mg2+ stężenie dla każdej matrycy i startera.
A-4 dNTP
—— Stężenie dNTP jest zbyt wysokie —— Odpowiednio zmniejsz stężenie dNTP
A-5 Temperatura wyżarzania
——Zbyt niska temperatura wyżarzania ——Odpowiednio zwiększyć temperaturę wyżarzania
A-6 cykli
——Zbyt wiele cykli ——Zoptymalizuj liczbę cykli

Pierwszym krokiem jest wybór odpowiedniej polimerazy. Zwykła polimeraza Taq nie może dokonać korekty ze względu na brak aktywności 3'-5' egzonukleazy, a niedopasowanie znacznie zmniejszy wydajność wydłużania fragmentów. Dlatego zwykła polimeraza Taq nie może skutecznie amplifikować fragmentów docelowych większych niż 5 kb. Polimerazę Taq ze specjalną modyfikacją lub inną polimerazę o wysokiej wierności należy wybrać w celu poprawy wydajności wydłużania i zaspokojenia potrzeb amplifikacji długich fragmentów. Ponadto amplifikacja długich fragmentów wymaga również odpowiedniego dostosowania projektu startera, czasu denaturacji, czasu wydłużania, pH buforu itp. Zwykle startery o wielkości 18-24 pz mogą prowadzić do lepszej wydajności. Aby zapobiec uszkodzeniu matrycy, czas denaturacji w 94°C należy skrócić do 30 sekund lub mniej na cykl, a czas wzrostu temperatury do 94°C przed amplifikacją powinien być krótszy niż 1 min. Ponadto ustawienie temperatury wydłużania na około 68°C i zaprojektowanie czasu wydłużania na poziomie 1 kb/min może zapewnić skuteczną amplifikację długich fragmentów.
Wskaźnik błędu amplifikacji PCR można zmniejszyć, stosując różne polimerazy DNA o wysokiej wierności. Spośród wszystkich dotychczas znalezionych polimeraz DNA Taq, enzym Pfu ma najniższy wskaźnik błędów i najwyższą wierność (patrz załączona tabela). Oprócz selekcji enzymów, naukowcy mogą jeszcze bardziej zmniejszyć szybkość mutacji PCR poprzez optymalizację warunków reakcji, w tym optymalizację składu buforu, stężenia termostabilnej polimerazy i optymalizację liczby cykli PCR.
Kategorie produktów
DLACZEGO WŁAŚNIE MY
Od momentu powstania nasza fabryka opracowuje produkty pierwszej światowej klasy, przestrzegając zasady
najpierw jakość. Nasze produkty zyskały doskonałą renomę w branży i cenne zaufanie wśród nowych i starych klientów.